クライオ電子顕微鏡法
我々の研究室では、鞭毛の様に非常に複雑で多種類の分子からなる巨大な生体分子複合体を、クライオ電子顕微鏡を使って高解像度で観察することを目標としています。研究対象である軸糸(鞭毛や繊毛のコアになる部分)の直径は約 260 nm で、光学顕微鏡の解像度では内部の複雑な構造を見ることが出来ません。そこで、軸糸の中の個々の分子の様子を明らかにするためには、光学顕微鏡よりも解像度が高く、生体試料の構造を三次元でそのまま観察出来るクライオ電子顕微鏡による観察が必要となります。
日本のクライオ電子顕微鏡を使う研究者・使いたいと考えている研究者の為のメーリングリストをgoogle groupsに作りました。参加はどなたでも可能です。 また、同様の目的のslackも立ち上げています。参加ご希望の方は mkikkawa あっと m.u-tokyo.ac.jp までメールを下さい。
クライオ電子顕微鏡の共用施設

創薬等先端技術支援基盤プラットフォームの構造解析ユニットとして、クライオ電子顕微鏡が利用可能です。
詳しくは、創薬等先端技術支援基盤プラットフォームのサイトをご覧下さい。
我々の研究室は、構造解析ユニット(構造解析領域)として、クライオ電子顕微鏡技術による支援と技術の高度化を行っています。
本施設の利用については、このリンクをご覧下さい。
クライオ電子顕微鏡法で何ができるのか?
クライオ電子顕微鏡法は、生体内の構造を染色することなく生のまま凍らせて観察する方法です。従って、「クライオ電子顕微鏡」という顕微鏡があるわけではなく、高性能な透過型電子顕微鏡(Transmission electron microscopy, 通常 TEMと略称されます)に、低温(-160 ~ -270度) のまま観察出来る装備(クライオホルダーや、試料汚染防止装置)を備えたものです。
日本のクライオ電子顕微鏡を使う研究者・使いたいと考えている研究者の為のメーリングリストをgoogle groupsに作りました。参加はどなたでも可能です。 また、同様の目的のslackも立ち上げています。参加ご希望の方は mkikkawa あっと m.u-tokyo.ac.jp までメールを下さい。

では、クライオ電子顕微鏡法を使うと何が出来るのでしょうか?
写真の例を以下に示します。(当研究室で撮った微小管の写真です。)
見ておわかりのように、非常にノイズの多い、何が写っているのかよくわからない写真です。
このような写真になる理由は、当てることの電子線量が非常に低いからです。具体的には、高解像度の写真を撮る場合には1Å平方あたり10電子程度になります。これ以上の電子線を当てると、試料が「焼けて」しまい、元の構造を保てなくなってしまいます。電子線による試料の損傷を防ぐため、非常に暗い「光」(実際には電子線です)でしか照らしておらず、そのため、シグナル(試料の構造)に比べて、ノイズ(主に、ショットノイズ)が大きくなります(S/Nが低い)。
そこで、何らかの方法でノイズを減らす必要が生じます。
そのためには、同じ形をしている分子や構造の電子顕微鏡像を数多く集め、画像処理によって、数千から数万の分子の平均像を使うことでS/Nを上げるのです。
この時に、いろいろな角度から見た画像を組み合わせることで、試料の三次元構造を観察する事が出来ます。
クライオ電子顕微鏡法の急速な発展(2012年~)
現在急速にクライオ電子顕微鏡法が広まりつつあります。これは、クライオ電子顕微鏡法が1980年代に誕生してから積み上げられてきた以下の様な技術
- 試料の急速凍結法
- 大量の画像から三次元構造を再構成する手法・ソフトウエア
- 電子顕微鏡の性能向上
- 安定なクライオステージの開発
- 電界放射型電子銃(Field emission gun)
- 電顕によるデータ収集の自動化
に加えて、Direct electron detector(電子線直接検知型・超高速CMOSカメラ)が開発されたことによります。これによって、結晶化していない生体試料からも、解像度3Å程度の構造を得ることが出来るようになり、アミノ酸や核酸の配列をもとにした原子モデルを組み立てることが可能になったからです。
このことは、PDBに登録されている原子モデルの数にも顕著に表れています。以下に示すのは、X線結晶解析、NMR、電子顕微鏡のそれぞれによって解かれデータベースに登録されている原子モデルの数ですが、2012年を境にして、グラフの傾きが大きく変化していることが読み取れます。この他にもクライオ電子顕微鏡に関する様々なグラフは Protein Data Bank in Europeの EMDB statisticsから見ることが出来ます。
PDBに登録されている原子モデルの数(縦軸はlogスケール)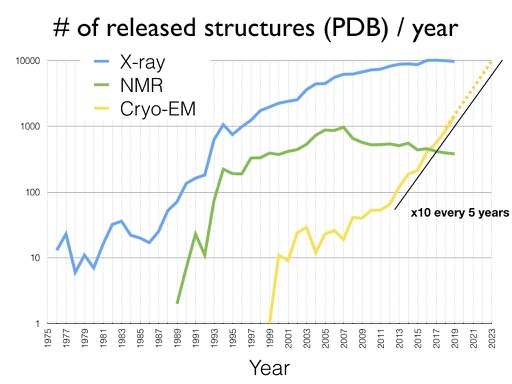
例えば、EMDBからリリースされるmapの数は以下の様に推移しています。(https://www.ebi.ac.uk/pdbe/emdb/statistics_num_res.html/)
